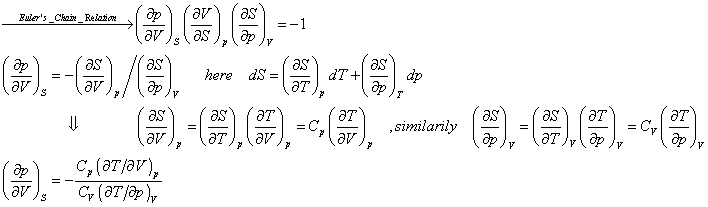1)次の反応に関する標準反応エントロピー![]()

2)
25℃、1atmでの純水、純エタノールのモル体積は、それぞれ18[cm3/mol], 58[cm3/mol]である。25wtモル%の水溶液の密度が0.92[g/cm3]、その時の水の部分モル体積が17.4[cm3/mol] のときのエタノールの部分モル体積を計算し、その値と純成分の値とを比較して差の要因について考察せよ。基礎物化 中クイズ ID( )Name( ) 2002.719
(回答は丁寧に。途中経過を省略しないこと、裏も使用可)
1)次の反応に関する標準反応エントロピー![]()

2)
25℃、1atmでの純水、純エタノールのモル体積は、それぞれ18[cm3/mol], 58[cm3/mol]である。25wtモル%の水溶液の密度が0.92[g/cm3]、その時の水の部分モル体積が17.4[cm3/mol] のときのエタノールの部分モル体積を計算し、その値と純成分の値とを比較して差の要因について考察せよ。 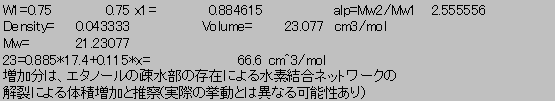
3)理想溶液とはどのような溶液をさすのか、説明せよ。
理想溶液の場合の混合Gibbsエネルギーはどうなるか?2成分系を例として表記せよ。
また、その理由を現象論的に説明せよ。
理想溶液とは、混合により 完全に相互溶解し、その際の体積変化もなく、温度変化もない。
(ΔG<0, ΔV=0 ΔH=0) あるいはラウール則の全組成範囲での成立
生成された溶液の組成をx、1-xとすると
![]()
溶解という現象が自発的に発生するため、ΔS≧0、ここで混合により、無秩序性が増加するのは明白であり、その結果エントロピーは増加するが、その寄与がxlnx+(1-x)ln(1-x)ということになる。
4)水の融解熱、蒸発熱が、それぞれ6kJ/mol, 40.6kJ/molとするとき、以下の設問に答えよ。
①通常凝固点の両側での化学ポテンシャルの温度に関する勾配![]() を求めよ。
を求めよ。
②通常沸点の両側での化学ポテンシャルの温度に関する勾配![]() を求めよ。
を求めよ。
③水を-5℃まで過冷却させたときの化学ポテンシャルは、同温での氷の値とどれだけ差があるか?
また、その結果から自発的な現象について考察せよ。
①:![]()
②:![]()
③: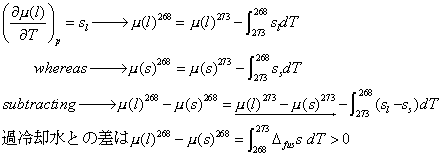
過冷却での化学ポテンシャル勾配が大きい。すなわち、何かの影響ですぐ凍る
5)ある気体を可逆的に断熱膨張(等エントロピー膨張)させたときの体積―圧力を予測したい。すなわち、![]() を求めたい。しかし、等エントロピー下でのp-
を求めたい。しかし、等エントロピー下でのp-